MayraB.C.Maymone,DDS,MD,DSc,aRobertO.Greer,DDS,ScD,LaurenK.Burdine,AnhDao-Cheng,SamanthaVenkatesh,PriyaCherukuriSahitya,AlexandreC.Maymone,DDS,JefferyKesecker,DDS,andNeelamA.Vashi,MDBoston,Massachusetts,andDenver,Colorado本期负责人:医院审校:周炳荣南京医院翻译:阳医院全文学习目标完成此项学习活动后,参与者应能够识别常见口腔黏膜良性肿瘤的主要临床特征;正确识别临床良性口腔黏膜病变;并选择每个特定病变的最合适的治疗。声明存在多种多样的口腔粘膜良性病变,表现为单独的口腔表现或与皮肤病相关。口腔病变可能彼此非常相似;因此,临床医生必须能够识别鉴别良恶性疾病的特征,并在必要时活检以辅助诊断。本系列继续医学教育的第一篇文章回顾了口腔解剖,口腔良性病变的临床特征,以及合适的管理和治疗方法。(JAmAcadDermatol;81:43-56.)关键词:口腔良性病变;良性色素性病变;颗粒细胞瘤;神经纤维瘤;神经瘤;口腔血管瘤;外周性巨细胞肉芽肿;周围骨化性纤维瘤;生理性色素沉着;化脓性肉芽肿。引言存在多种多样的口腔粘膜良性病变,表现为单独的口腔表现或与皮肤病相关。口腔病变可能彼此非常相似;因此,临床医生必须能够识别鉴别良恶性疾病的特征,并在必要时活检以辅助诊断[1]。口腔基础解剖学关键点●口腔由唇粘膜、粘膜、颊粘膜、牙龈、舌前三分之二、口腔底和硬腭组成●口腔粘膜是一种复层鳞状上皮,其组织学变化与特定功能相适应。
口腔从唇一直延伸到口咽后部,包括3个主要区域:口腔本体、口咽和前庭。口腔本体是牙弓之间的区域,后面与腭舌弓相邻(图1)。口咽位于腭舌弓后面,由可见的咽后壁、腭扁桃体、舌后三分之一和软腭组成。前庭是牙列与嘴唇或脸颊之间的空间区域。前庭内,唇系带、上颌骨中线粘膜皱褶和下颌骨将嘴唇附着在较薄的牙槽粘膜和较厚的牙龈粘膜上[2]。
图1.口腔基本解剖。1,前庭;2,牙龈;3,口咽;4,悬雍垂;5,硬腭;6,磨牙后三角。
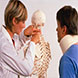
整个口腔的内壁是湿润的口腔粘膜,从面部皮肤的唇红处向外分开。口腔粘膜是一种可移动的鳞状层状非角化粘膜,是口腔颊部和口腔底的主要上皮类型。更持久的角化粘膜排列在舌头、牙龈和硬腭的背表面,以承受咀嚼的力量。口腔粘膜的非角化层约占口腔总面积的60%。咀嚼粘膜较硬,舌背粘膜较特殊,分别占舌粘膜的25%和15%。上皮细胞附着在下层结缔组织和骨膜上,以加强支持。口腔粘膜前体细胞在基底层内再生。口腔前庭和底部的粘膜在牙龈接合处与牙龈相连。口腔良性病变化脓性肉芽肿关键点●化脓性肉芽肿是一种常见的增生性反应性病变,由外伤、炎症、激素变化或药物引起●外科切除是标准治疗背景。化脓性肉芽肿(PG)是口腔内常见的良性血管炎性病变。PG这个词用词不当,因为这种病变不是由细菌引起的,也不是真正的肉芽肿。许多因素可能刺激PG的形成,包括创伤、慢性局部炎症、激素影响或药物治疗[4]。三分之一的PGs与外伤有关,约5%发生在妊娠期,最常见于妊娠中期或晚期。PG常见于女性和二十多岁的年轻人[5]。临床特征。PG呈红色到红紫色,表现为平滑的丘疹或结节,大小从几毫米到约2.5厘米不等[4]。病变可以是单发或多发,无蒂或有蒂(图2,A)。在PG稳定生长之前通常会有一段快速增长的时期[6]。创伤通常会导致PGs出血。最常见的部位是皮肤和口腔。口腔中约75%的PGs发生在上颌前牙龈、唇、舌和颊粘膜[5]。组织病理学检查显示肉芽组织增生,毛细血管扩张,充满红细胞,内皮细胞突起。这些小叶排列的毛细血管中会有炎症细胞,包括中性粒细胞、浆细胞和淋巴细胞(图2,B)。组织病理学检查有助于区分增生性牙龈炎、卡波西肉瘤、周围骨化纤维瘤和外周性巨细胞肉芽肿[7]。
图2所示。化脓性肉芽肿。上颌粘膜充血性息肉样病变(黑色箭头)。粘膜结节,被角质化的鳞状上皮覆盖,由疏松的网状胶原和肉芽组织支撑。肉芽组织由扩张的血管网、急慢性炎症细胞、出血和蛋白质碎片组成。(A,由DDS的JohnMcDowell提供。)管理。对于PG,建议手术切除周围边缘2毫米,直至骨膜或致病体[4]。应检查病变周围是否有任何刺激物,并对局部牙列进行评估,以确定是否有牙菌斑、牙石、异物或可能导致过度炎症和复发的缺陷,其发生率为16%[6]。病例报告显示,PG的新疗法取得了成功,包括使用Nd:YAG激光治疗[8,9],具有较低的出血风险、可止血,并无不良事件。其他的案例研究建议使用脉冲染料激光器[10]、冷冻手术、乙醇注射、硫酸十四烷基钠硬化治疗(证据水平,V)[13]。外周性骨化性纤维瘤关键点●外周性骨化纤维瘤是牙周韧带内成纤维细胞和牙源性上皮细胞巢的反应性增殖●外周性骨化纤维瘤的治疗包括牙龈病变的完全切除和手术修复背景。外周骨化纤维瘤(POF)是一种由牙周韧带细胞增生引起的口腔增生性反应性病变。如果不及时治疗,POF会导致严重的骨质流失和牙齿损伤。POF被认为是创伤引起的细胞增殖的结果,与反应性营养不良钙化和骨生长有关。约60%的POFs累及上颌牙龈,其中约50%位于前切牙和犬牙区[14]。传统上,POF被发现在10到29岁的女性中最为普遍,这可能是由于激素的影响。然而,最近的一项文献综述表明,男性患POF的几率也与女性相似[15]。POF可能有多基因起源,但关于特定基因的突变却很少报道。临床特征。疼痛和局部充血是POF的典型症状。病变通常直径小于2厘米,但可以长到10厘米大[14]。病变大小不代表总生长时间,可发生多发病变[15]。POF患者通常表现为牙龈粘膜红肿、局部肿胀,根据病变大小,可伴有溃疡和牙齿松动(图3,A)。组织学检查,POF将包含钙化和内皮细胞增殖增加,成熟的胶原和成纤维细胞组织带(图3,B)。鉴别诊断包括PG、外周巨细胞肉芽肿(PGCG)和牙龈纤维瘤。
图3.外周性骨化性纤维瘤。结节性息肉样生长,从牙间乳头延伸至尖牙和第一颗双尖牙之间。角化鳞状上皮,由成熟结缔组织和纤维组织带支持。聚集在纤维结缔组织基质内的骨结节性聚集物(黑色箭头)。C,骨聚集体的高倍图像。(A,由DDS的JohnMcDowell提供。)管理。POF治疗的标准治疗是完全的局部切除,包括边缘的2毫米健康组织和受影响的牙周膜和骨膜的切除,因为据报道复发率在16%到28%之间[6,16]。POF可影响附近的牙列,拔牙时应考虑刮除(去除牙菌斑和牙石)和牙根刨平(平滑牙根表面)以消除复发[16,17]。外周性巨细胞肉芽肿关键点●外周性巨细胞肉芽肿是破骨细胞源性反应性病变●诊断基于纤维血管基质中巨细胞的独特组织学表现●切除是治疗的选择背景。PGCGs是牙龈或粘膜的反应性口腔病变。它们被认为来自破骨细胞或单核吞噬细胞。女性的患病率是男性的两倍。发病年龄因性别而异。女性和男性分别在50多岁和20多岁受到影响的可能性最高[18]。临床特点。PGCG的外观变化很大。病变通常是软的,海绵状的,容易出血[6]。病变的颜色通常是红色,但病变也可能出现紫色、蓝色、粉红色、棕色或白色。虽然它们可能出现在口腔的任何地方,但最常见的位置是切牙和犬齿区域,与上颌骨相比,累及下颌骨的可能性更高(图4,A)。PGCGs大小不等,多数病变直径小于2cm[19],生长迅速和溃疡与损伤的反复创伤有关[6,18]。PGCGs的临床表现与PG和POF相似[20]。组织学检查显示大量多核巨细胞散布在增殖的梭形和卵球形间充质细胞之间。病变可能表现出广泛的毛细血管生长(图4,B)。复层鳞状上皮表面会很明显,并且经常溃烂。可出现急性和慢性炎症细胞和出血[20],伴有含铁血黄素沉积[6]。35%的病灶可见钙化组织[20]。
图4.外周巨细胞肉芽肿。累及下颌牙龈的局部出血性结节占据了侧切牙的四分之三。B,多核巨细胞位于疏松的网状胶原和肉芽组织基质中。肉芽组织由扩张的血管网、内皮细胞、蛋白质碎片和出血组成。(A,由DDS的JohnMcDowell提供。)管理。早期诊断PGCG是至关重要的,以尽量减少手术治疗的必要性,以减少并发症,如骨暴露,牙齿移位,或骨丢失[19]。X线检查可以帮助确定病灶的来源和边界[21]。PGCG在儿童患者中具有比成人更快的生长速度。复发是常见的[18]。手术切除病变是主要的治疗选择(证据级别,V)。切除完成时,手术边缘距周围2至5毫米。应特别注意去除可能导致PGCG的骨膜或牙周韧带。如果病变和任何局部刺激物被完全清除,复发率将会降低到1.4%到12%不等。发生在种植牙体附近的病变有较高的复发几率[20]。颗粒细胞瘤关键点●颗粒细胞瘤起源于施万细胞,由于溶酶体的存在而在组织学上呈颗粒状●颗粒细胞瘤通常是良性的,但有1%至2%的病例发生恶性转化●外科切除是治疗手段背景。颗粒细胞瘤通常是良性的神经肿瘤。其颗粒状的组织学表现可归因于溶酶体囊泡的改变。这些病变占所有软组织肿瘤的0.5%[22]。它们起源于施万细胞,可能由轴索损伤后的瓦勒氏变性引起[23]。女性发生的几率是男性的两倍。患病率在20至40岁的人群中最高[6]。这些肿瘤中,只有不到2%可能会变成恶性肿瘤;然而,这些肿瘤往往出现在下肢,位于头颈部的肿瘤极为罕见。恶性肿瘤5年生存率为62.8%[22]。临床特征。大约40%的GC肿瘤出现在口腔。舌头是最常见的部位。病变通常是无痛的,摸起来很硬。颜色可能不同,病变可能呈黄色,白色,或苍白的外观(图5,A)。在大约10%到15%的患者中,会出现1个以上的病变。正常情况下,肿瘤的直径限制在2厘米左右,但病变可能会变大(小于等于12厘米),特别是当它们变成恶性时。组织学检查,肿瘤没有包膜。上皮可能正常或呈假上皮瘤样增生。肿瘤细胞呈多边形或圆形,细胞核小,胞质嗜酸性,胞质颗粒。肿瘤细胞呈片状或簇状排列,由结缔组织和骨骼肌纤维分开(图5,B)[6,24]。
图5.颗粒细胞肿瘤。结节状、可自由活动的病变,累及舌背表面。巢状、索状和片状的大细胞,细胞核和颗粒状细胞质染色较深。这些细胞位于疏松的网状胶原基质中。管理。对于良性肿瘤,目前公认的治疗方法是手术切除,直到病灶周边5毫米边缘。GC的复发率约为7%。复发性肿瘤往往是新发肿瘤,而不是源于以前的病变(证据水平,V)[6]。目前,对于那些极其罕见的转移性GC,还没有有效的治疗方法。在一项案例研究中,有1位患者对酪氨酸激酶受体抑制剂帕唑帕尼治疗有反应(证据水平,V)[25]。口腔血管瘤关键点●口腔血管瘤是一种常见的良性肿瘤,典型的自愈性肿瘤。●管理主要是观察;然而,可以通过手术来去除肿物背景。口腔血管瘤是常见的良性肿瘤,最常见于婴幼儿。女性血管瘤的发病率是男性的3倍。婴儿血管瘤的危险因素包括早产和低出生体重。病因目前尚不清楚;然而,肿瘤与高于正常浓度的CD、血管内皮生长因子A和环氧合酶-2之间存在相关性[26]。临床特征。头颈部是血管瘤最常见的发病部位,占60%[27]。血管瘤特征性表现为大小不等的鲜红色丘疹或结节(图6,A)。肿瘤开始于快速增殖期,持续6-8个月。在组织病理学上,这一阶段的特征是内皮细胞增生和多层基底膜的形成(图6,B)[27]。大多数病灶在3-5个月内达到最大体积的80%。增殖阶段之后是缓慢的消退阶段。此阶段的组织病理学特征包括纤维化、脂肪沉积和病变消退[27]。
图6.口腔血管瘤。A.左颊粘膜边界清楚的紫色结节。B.粘膜结节,被角化的鳞状上皮所覆盖。上皮细胞由真皮疏松的网状结缔组织支撑。在浅表结缔组织中可见内皮细胞衬砌的扩张的血管。这些血管毗邻上皮的基底层。(A,由DDS的JohnMcDowell提供。)图7.神经纤维瘤。A.单发、边界清楚的结节性病变,累及舌侧缘。B、梭形细胞增殖。梭形细胞有伸长的嗜碱性细胞核和极少量的嗜酸性细胞质。这些细胞通常在丛生的结缔组织间质中呈丛生状排列。(A,由DDS的JohnMcDowell提供。)管理。大多数血管瘤在没有治疗的情况下可自愈。大约10%到20%的病人需要治疗[28]。治疗方法包括烧灼疗法、冷冻疗法、激光疗法、放射疗法、硬化疗法和外科手术[29]。硬化治疗和激光治疗是最常见的选择。硬化剂有很高的反应率,成本较低,而且容易获得[30]。有文献记载,使用3%的十四烷基硫酸钠经病变周围和中央注射是有效的(证据水平,iv)[30]。硬化治疗可导致12%-30%的患者皮肤和软组织损伤(组织刺激和血栓形成),10%的患者出现非永久性神经病变[31,32]。激光治疗已被证明是一种有效的治疗选择,包括黄光激光器(-纳米;证据水平,V)和Nd:YAG激光(证据水平,IV)[32]。潜在的不良反应包括组织剥脱和瘢痕[31,32]。神经鞘源性肿瘤:神经纤维瘤和神经瘤关键点●口腔周围神经鞘良性肿瘤包括外伤性神经瘤、神经纤维瘤、神经鞘瘤和栅栏状包膜神经瘤。●病变通常是良性的,但可能与其他疾病有关,并可能有恶性转化的危险。●病变的诊断根据组织学表现,治疗包括手术切除。背景。神经源性口腔肿瘤很少见,口腔周围神经鞘肿瘤仅占口腔病变的0.2%[33,34]。这些肿瘤通常是良性的,但它们的存在可能预示着其他疾病和一些病变具有恶性转化的风险。肿瘤可能是反应性的,发生在对神经损伤的反应中,或者它们可能有真正的肿瘤起源。临床特征。口腔周围神经鞘良性肿瘤包括外伤性神经瘤、神经纤维瘤、施万细胞瘤或神经鞘瘤,以及栅栏状包膜神经瘤或孤立的局限性神经瘤[34]。外伤性神经瘤是一种非肿瘤性过程,发生于神经损伤后,组织学上由增生的施万细胞和轴突组成[35,36]。施万细胞瘤是起源于施万细胞的肿瘤性病变。它们很少在口腔内发现,占所有口腔内病变的0.04%[33,37]。肿瘤最常见于30-40岁的患者,恶性转化的发生率在8%到13.9%之间[38]。神经纤维瘤是最常见的外周神经鞘肿瘤,在所有口腔外周神经鞘肿瘤中,报告的发生率分别为20.8%和32%(图7,A)[33,39]。与神经纤维瘤病(NF1)相关的孤立性神经纤维瘤发生恶变的风险较低[40,41],有NF1基因的个体有2%到6%的肿瘤恶性转化风险[42]。神经纤维瘤的丛状变异被认为是NF1的病理学特征,当与NF1相关时,可表现为疼痛、神经缺损和更高的恶性转化风险[42]。由于这些肿瘤的临床表现与其他肿瘤相似,诊断需要获得活检标本和组织病理学评估(表I)[33,35]。
表I.神经鞘源性肿瘤的一般特征及临床特点NF1,神经纤维瘤;;PEN,栅栏状神经瘤。管理。手术切除是大多数周围神经鞘肿瘤的推荐治疗方法。神经鞘瘤和栅栏状神经鞘瘤切除后复发的病例很少[37,38,43]。神经纤维瘤手术切除后复发率低;然而,通常与NF1相关的较大病变复发的风险更高(证据水平,IIIA)[42]。在较年轻的患者中,孤立性神经纤维瘤的存在可能提示NF1,因此推荐年龄小于20岁且存在孤立性神经纤维瘤复发的患者进行遗传检测[43]。生理性色素沉着关键点●生理性色素沉着以口腔粘膜弥漫对称性色素沉着为特征●根据临床表现诊断,无需治疗背景。生理色素沉着(PH)的特征是口腔粘膜弥漫性对称色素沉着[44],最常见的是牙龈。已知的影响色素沉着程度的因素是黏膜角化程度、血管形成程度、口腔黑素体的大小和黑素化程度以及黏膜下组织的质量[45]。PH在肤色较深的个体中更为常见,而且对男性和女性的影响是一样的。患病率随研究人群而异[46]。临床特征。PH呈弥漫性均匀分布的褐色沉着(图8),通常累及附着的牙龈,然后是颊粘膜、唇粘膜、舌头和上颚[46]。PH可在婴儿期出现,并被认为随着青春期的到来而增加或变暗。与皮肤黑色素细胞相似,口腔黑色素细胞产生的黑色素量受遗传背景的影响,色素沉着强度可能受物理、化学和激素因素的影响[47]。
图8.生理性色素沉着。广泛的牙龈色素沉着,对这个非裔美国人的病人来说是正常的。(由DDS的JohnMcDowell提供)PH的诊断是建立在排除其他弥漫性色素沉着疾病的基础上的,包括吸烟者的黑色素沉着病、艾迪生病、血色素沉着病、药物引起的、局灶性色素沉着病,如银汞合金文身、口腔黑色素斑、口腔黑色素瘤和炎症后色素沉着。组织病理学表现为基底层和真皮浅层黑色素增多、黑色素失禁、噬色素细胞增多。这些特征与吸烟者的黑变病和口腔黑变斑疹有共同之处[48]。管理。需要对口腔粘膜表面进行彻底检查,以将PH与其他异常色素沉着疾病区分开来,特别是在最近开始出现色素沉着过多的情况下。不需要治疗;然而,如果患者有需求的话,使用冷冻疗法[49]和ND:YAD激光可以有效治疗(证据水平,V)[50]。良性色素性病变关键点●良性色素性病变可能有内在或外在的病因。●口腔色素沉着可能是局部性的,或是系统性疾病的一部分表现。●适当的临床评估需要彻底的病史采集和体格检查,对于不确定的病变,应进行活检。背景。口腔色素性病变比较常见,可能是生理性或病理性的[51]。它们可以通过几种方式进行分类,包括黑色素细胞病变与非黑色素细胞病变、内在色素沉着与外在色素沉着、局灶性色素沉着与弥漫性色素沉着(图9)。口腔内色素沉着可以有一个大的诊断模式,从局部反应过程到更与全身性疾病相关的表现[52]。适当的临床评估需要详细的病史,详细的体格检查,以及在获得活检标本后可能的进一步评估[45]。
图9.良性病变的诊断流程。临床特征。良性色素性病变的弥漫性/双侧色素沉着特征见表II。Peutze-jeghers综合征。Peutze-jeghers综合征是一种常染色体显性遗传综合征,其特征是嘴唇或口周弥漫性色素沉着斑。其他有口腔表现的遗传性皮肤病见表III[53]。表II.口腔粘膜弥漫性/双侧良性色素沉着的特点
ACTH,促肾上腺皮质激素;MSH,黑素细胞刺激素表III.口腔遗传性皮肤病[70]
由Wilder等更新。[70]Addison病。原发性肾上腺功能不全的患者,由于促肾上腺皮质激素的增加,口腔粘膜可能出现棕色斑块[53]。重金属。口腔粘膜色素沉着可由血清铅等金属水平升高引起。色素沉着通常表现为沿牙龈边缘的一条蓝黑色线,称为Burtonian线。药物导致的。药物或代谢物沉积在口腔上皮和真皮可能引起色素性病变。病变多见于腭部和牙龈[51]。炎症后。急性或慢性炎症变化可导致色素改变[54]。吸烟者的黑变病。以口腔黏膜弥漫性褐色黄斑变性为特征,吸烟者的黑变病最常累及下颌前唇黏膜[53]。局部色素沉着特征如表IV所示。雀斑。雀斑是一种常见的褐色至棕色斑点,由于日晒引起的黑色素生成,常出现在曝光部位的皮肤上[53]。唇黑斑。唇黑斑是年轻成年女性下唇常见的小而均匀的色素性斑疹(图10)[55]。这些病变以前被归类为雀斑样痣[56]。
图10.唇黑斑。单一,界限清楚,在唇红边缘均匀的棕色斑点。银汞合金纹身。银汞合金纹身是在牙科治疗过程中,由于银汞合金修复材料沉积到口腔粘膜而导致的蓝黑色斑点(图11)[53]。
图11.银汞合金纹身。颊粘膜上的一种边界清楚、色素沉着的病变。注意银汞合金填充物的位置。椭圆形异物被角化鳞状上皮所覆盖,由含有弥漫性慢性炎症浸润的胶原所支持。浸润物内包裹有色素沉着的异物,与银汞合金一致,银汞合金偶尔被多核巨细胞和组织细胞包围。(A,由DDS的JohnMcDowell提供。)口腔黑色素棘皮瘤。口腔黑色素棘皮瘤表现为棕色/黑色界限清楚的斑点或丘疹,是咀嚼或外伤的反应[57]。口腔黑色素细胞痣。口腔黑色素细胞痣是由上皮细胞或结缔组织内的痣细胞堆积而形成的清晰可见的斑疹或丘疹(图12)[58]。
图12.口腔黑色素细胞痣。颊粘膜上的一个单一的、边界清楚的、浅色到黄褐色斑点。(由DDS的JohnMcDowell提供)管理。口腔黏膜病变的诊断和治疗可能对临床医师具有挑战性。通常,临床病史和检查可能足以正确识别病变。然而,对于不确定的病例,可能需要进行更广泛的检查,以便作出明确的诊断。皮肤镜检查是一种可用的非侵入性方法,可用于评估可疑的病变,表IV归纳了鉴别孤立病变的常见特征[59]。反射共焦显微镜是另一种无创性的方法,有可能区分恶性和非恶性病变,但这项技术由于缺乏既定的指南而受到限制[60]。诊断口腔粘膜病变的金标准是获得口腔活检标本[61]。活检标本对于局灶性病变有特殊的用途,通常活检标本应该从怀疑有黑色素瘤和快速生长的病变中获得[45]。对于弥漫性病变,活检标本的效用较小,可能有非特异性的发现。在这些情况下,可能需要通过实验室研究对系统进行审查,以确定诊断[61]。表IV.口腔粘膜局灶性良性色素沉着的特点总之,口腔黏膜病变的诊断是临床实践的重要组成部分。口腔病变是相对常见的疾病,但临床医生可能会发现,很难区分良恶性病变。引起口腔粘膜肿瘤和其他病变的原因包括外部因素、反应过程、系统性疾病和肿瘤进展。对可疑病例进行彻底地病史采集和适当的检查可能能够得出一个令人信服的诊断。然而,对于许多肿瘤和涉及粘膜的口腔色素性病变,获得活检标本可能具有诊断价值[1,61]。参考文献略


 当前时间:
当前时间:  E-Mail:
E-Mail: